�Ϻ����̼��g\��h��������h��W�ϰl������-�����x��-��ˮ����������3D��ӡ
��Ѫ�Ǽ����T�������������h��������ȱ�p���ޏ�����˾�������Ϻ����̼��g��W��ͬ�R���ڈFꠡ���h������W���tɏ���ڈF���h��W�����tԺ�����ڈF����_�l��һ�N��������ȱ�p�ޏ͵�����TZGP (α-TCP/ZnO/GM@P2) �ͺ�֧����ԓ��������: "A Triple-Integrated 3D-Printed Composite Scaffold of High-Activity Peptide-Metal Ion-Bone Cement Facilitates Osteo-Vascular Regenerative Repair of Diabetic Bone Defects" �l����ADVANCED FUNCTIONAL MATERIALS�ϡ������Y��������α-TCPˮ��֧�ܡ�ZnO�{���w����ؓ�d�ͱ��oP2 (һ�N���ͼנ����ټ������P��) �����z�F�˻��a�ă��ݡ�TZGP֧���ڝM�����|�ǵęCе����Ҫ���ͬ�r�����a�˟o�C֧������������ĵIJ��㡣�������������Եõ�����������֧�ܾ��п����Ϳ��������ԡ��w����w�ȽY��������TZGP֧��ጷŻ�������P2��Zn2+���ڸ��������h���д��M������ֳ��ļ�����p�ټ����������e�ۣ�����DNA�p���;����w���B�����T���ɹ�Ѫ�����ɷֻ����c���y��α-TCP ֧����ȣ�TZGP֧�ܱ��F�������������オ���ԣ����پֲ��M����ӯ�����M����ȱ�p�ĹǶѷe��Ѫ���ؽ�����ˣ�TZGP֧�ܵ��·f�OӋ���Ԟ��ޏ�����ȱ�p�ṩ��һ�N����ǰ;�ķ�����

һ��������B
����(DM)�dz�Ҋ������ȫ��ʮ��֮һ�����˻���������ȫ���Դ��x�ȷ����Ɂy���������Ը�Ѫ�Ǟ����������l�Ǵ��x�{�������_ʧ�{�Ȳ����h��׃�����ƉĹǴ��x���������ӹ��|���ɺ��۰l���ʣ�߀���¾����w�����ϵK���o�����߹�ȱ�p�����ޏ͎�������
�ڹǽM�������У������}�dz��õĹ�ȱ�p�ޏͲ��ϣ���α-�������}(α- TCP)��ˮ���β -�������}(β-TCP)�џ�֧�ܣ��������������á�����TCP�����オ�������ޡ��Cе���ܲ��ѡ����T���Բ��㡢ȱ����Ѫ�ܘ������ӣ��y�Դ��M�����߹�ȱ�p���ϡ�β-TCP֧�ܿ��џ����Y�Ƃ䣬ˎ��ؓ�d�����Ϳ�ӣ�����ˎ��ጷ����ͳ��m�r�g��α-TCP���オ������ո��죬�Ҝ����c������Һ�w���|�������γ��}��ʯ���ṩ�Cе���ȣ�߀�����Ӝ���ˎ�����������ጷŵ����������|�������ޏͣ����о����������\�{������(ZnONPs)�{�� pH ֵ���併��a���� Zn²⁺߀�ܴ��M�ɹǡ�
�נ����ټ���(PTH)���c���D�����}�״��x���д��M���γɡ�Ѫ�ܻ��������յ����á��R����Ҫ���g��Ƥ��ע��ȫ���oˎ���s���ڄ�����˥�ڶ̡��ֲ�ˎ�����y�S�֡��ֲ��������Ȇ��}��ǰ���о��l�F��PTH���P��-2(P2)�ɵͳɱ������ϳɡ��cPTH (1-34)��ȣ�P2�}�M���^�������������ֲ�ˎ������r�g�L��߀�ܱ���ˎ��ͻ�lጷŌ��µĸ߹����ա����湦�ܻ���P2֧�ܲ��ϣ��ɹǺ�Ѫ�������T��������PTH (1-34)���ã��ƹǼ����ֻ������^�������ڹ����۷e�����^��ֱ�Ӱ�P2�����ˮ�����Ɖ���Y���ͻ��ԣ��y����Ч�dˎ���������z���z(GMs)����P2�f���d�w�������o�Ϳ���P2ጷŵ����á�
���о��M����α-TCP-ZnONP-P2�ͺϵ��²��ԣ�����،��ЙC�����ġ��o�C֧�ܺͽ����x��������һ���Ƃ��һ�N���͵�3D��ͺ�֧��(TZGP֧��)���IJ��ϽM�ֵĽǶȿ���TZGP֧�ܸ��M�����ݻ��a���@���ظ����ˆμ�TCP֧�ܽ����ٶ�����ȱ����������ġ��������Խ���a��Ȳ������ء��IJ��Ϲ��ܵĽǶȿ��������ˆμ�TCP֧�ܽ�������ȱ��������ġ������Խ���a��Ȳ��㡣�ڹ����ϣ�TZGP֧�ܝM�����|�ǙCе����Ҫ�����������ԡ����オ���ԡ������ԺͿ�������������ɫ����ͨ�^����ijɹ� - Ѫ���������ã����M����ȱ�p���ޏ�(�D1)��
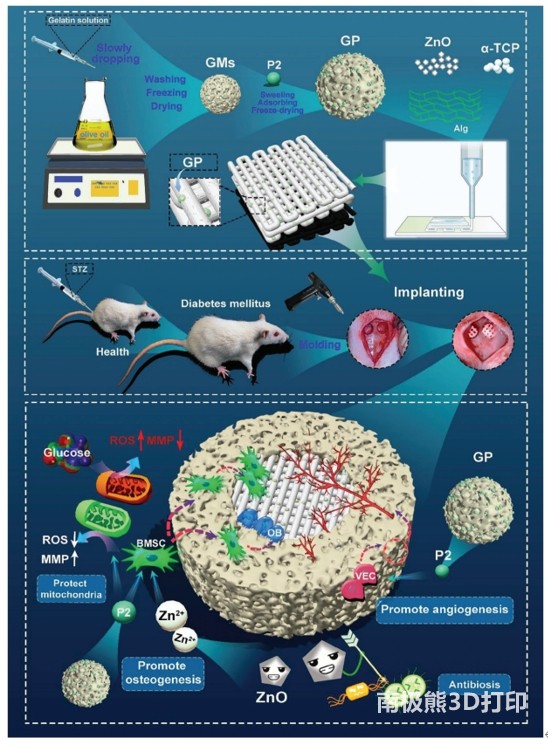
�D 1. ������-�����x��-��ˮ�����ؼ���3D��ӡ�ͺ�֧��ʾ��D��������ȱ�p�Ĺ�Ѫ�������ޏ͡�GMs�����z���z��P2���נ����ټ������P��-2��GP��ؓ�dP2��GM��Alg���������}��STZ����������أ�ROS����������MMP�������wĤ�λ��OB���ɹǼ�����BMSC�������g���|�ɼ�����VEC��Ѫ�܃�Ƥ������ ���������c����2.1 3D��ӡTZGP�ͺ�֧�ܵ�������α-TCP��ĩ(3g)��ZnONPs(2% w/v)��GMs(5% w/v)��GPs(5%w/v)����10% w/v Alg���z�С��M�ЙCе����ֱ���γɺ����ԫ@�ô�ӡīˮ��������1�еĽM���Ƃ��ķN��ͬ�ďͺ�֧�ܣ�T��TZ��TZG��TZGP֧�ܡ��ͺ�֧����3D��ӡ�C(SunP BioMaker 2)�ϴ�ӡ��3D��ӡ�C����ֱ����500 μm���ݗU�D���ٶȞ�0.5-1 mm3s-1����ӡ�ٶȞ�5-15 mm-1 s-1������ӡ�õ�֧��ë������10%������Һ��5����M�н�������Ȼ����ȥ�x��ˮ�_ϴ3�Σ�������ո������-20°C���档 �����Y��3.1 3D ��ӡ�ͺ�֧�ܵı������о���GM����P2��ˎ���f���d�w����3D��ӡ�ͺ�֧�ܵ��Ƃ��^���У���P2�ṩ���o����GM���Ƃ���D2A��ʾ����ǰ�����z��ĩ���^��ߴ�IJ�Ҏ�t�K��(�D2B)���ɹ��Ƃ��GM��Ҏ�t���������С�w��(�D2B)�� �����ֲ�������10–70 μm��������35–50 μm��ƽ��ֱ����41.33 ± 9.13 μm(�D2C)��α-TCP�o�����߹ǂ����Ժ�������ԣ��������տ졣TCP/ZnONP/GM (TZG)�ͺ�֧�����Ҝ��µ��Ƃ��^����D2D��ʾ����׃�yԇ�@ʾ���ӡ��ī��ճ�ȵͼ����������������ޏ������ͼ���׃ϡ���ԣ��߂�ɔD���ԺͿɴ�ӡ��(�D2E��2F)��X�侀����x(XRD)�Y�����������̵ļ�α-TCP(T)֧���е���Ҫ��������ʯ��TZ��TZG�ͺ�֧�ܵ��������c��TCP֧�ܵ������������ͬ���f��ZnONPs��GM�ļ��댦TCP�Ĺ̻��a��]��Ӱ�(�D2G)��T֧�ܵij�ʼ����a��������ԣ���ZnONP�ljA�����|�����cH+����ጷ�Zn2+���B�m pH�y��������ZnONP��������������TZ��pHֵ������TZG֧�ܡ�TZ��TZG֧�ܵ�pHֵ��T֧�ܸ��ӽ����Ժ������h��(�D2H)��Zn2+��ጷń����W������TZ��TZG֧����ǰ3�܃Ⱦ��ɷ���ጷ�Zn2+(�D2I)��TZG֧��ጷŵ�Zn2+����Ը���TZ֧�ܡ��B�m8�ܵĜyԇ�������������M֧�ܾ����F�������⡣�cT��TZ֧����ȣ�TZG֧�ܱ��F�����õĽ���Ч��(�D2J)���@�������������GM����TZG�Ľ����ٶ��Կ���TZ֧�ܡ�SEM�Y���@ʾ��TZG֧���S�r�g�������ΑB��֧�ܽ����֧�܃Ȳ���GM���@¶�������������ǽM���ṩ�����ͽ��Ŀ��g����ӡ֧�ܽ�����������Һ�аl�������̷�����֧���ṩ�˻����ęCе���ȡ���α-TCP�����^���У��ܽ��Ca2+���c֧���еĺ������c���ϣ��Mһ������֧�ܵęCе���ȡ�TZ֧�ܵĿ�������(23.34 ± 1.80 MPa)�cT֧��(24.17 ± 1.55 MPa)��ț]�����@׃������TZG�Ŀ�������(14.53 ± 1.27 MPa)�½��������@(�D2K)��GM��������ܕ�����֧�ܵ������ԣ������Ǐͺ�֧�ܙCе�����½���ԭ�����\���ǣ�����Ȼ�܉�M�����|�ǵ�Ҫ��(4-12 MPa)��ͨ�^�@�R�B�m�^��l�F��������ˮ��PBS�е�GMֱ������Ȼ����u���⣬28��Ƚ����ʳ��^90%���Hʣ�������w����ZnONPs�Ǐ�Ч����������ֱ�ӓp����������Ĥ�ϵĵ����|��֬�|�����¼��������ȃ�����й©��������ZnONPs��Zn2+߀���Դ��^�ܓp��Ĥ���Ɖļ����Ȳ����ܣ����¼�������������SEM�D��ZnONPs��ƽ��������30.33 ± 7.30 nm���ڱ��о��У�ͨ�^�Uɢ�巨��C��ZnONPs�������x��TZ��TZG֧��һ���Ŀ�������(�D2L)���@�������A������ȱ�p�еľֲ�������Ⱦ��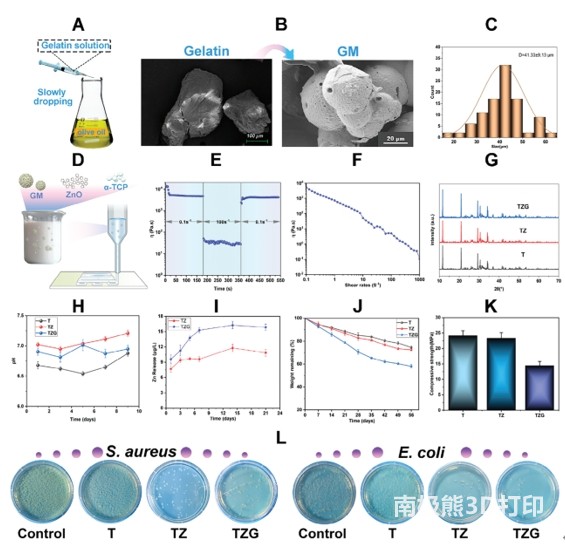 �D2. T��TZ��TZG֧�ܵı�����A) GM�Ƃ�ʾ��D��B)���z��GM��SEM��C) GM�����ȷֲ���D) TZG֧���Ƃ�ʾ��D��E��F) TZGīˮ����׃�yԇ��G) XRD��H) T��TZ��TZG֧�ܵ�pHֵ(n = 3)��I) TZ��TZG֧����Zn2+��ጷń����W(n = 3)��J)��������(n = 5)��K)��������(n = 5)��L) T��TZ��TZG֧�ܵĿ������ܜyԇ��
�D2. T��TZ��TZG֧�ܵı�����A) GM�Ƃ�ʾ��D��B)���z��GM��SEM��C) GM�����ȷֲ���D) TZG֧���Ƃ�ʾ��D��E��F) TZGīˮ����׃�yԇ��G) XRD��H) T��TZ��TZG֧�ܵ�pHֵ(n = 3)��I) TZ��TZG֧����Zn2+��ጷń����W(n = 3)��J)��������(n = 5)��K)��������(n = 5)��L) T��TZ��TZG֧�ܵĿ������ܜyԇ��
3.2 �ͺ�֧�ܵ������������о��l�F��ZnONPs��ͨ�^���·�������ܶ�չ�F�����������ԡ��ڱ��о��У�TZ �� TZG֧�ܵĵ����ɻ����������T֧���@����ߣ��f��ZnONPs�x��ͺ�֧�ܿ������ԡ�P2ؓ�dʾ��D��3A��ʾ������GM���ܽ��ԡ�����Ժ��������ԣ���P2����GM(GP)�С�P2��ƽ��ؓ�dЧ�ʞ�95.38% ± 1.37%��ͨ�^���ߟɹ��@�R���Կ���ؓ�d�Ю�������ɹ���(FITC)��ӛ��P2(P2FITC)��GP�l����������ľGɫ�ɹ�(�D3A)������GP��������Ҏ�t�����Ρ������~׃�Q�t����V(FTIR)�Y��������GM��GP����1700–1500 cm-1�^���γ��˃ɂ���ͬ������I������II�������⣬GP��1540��1453 cm−1̎����ӷ����ͻ�������Ҳ��������F��NH2�ēu�[��Ӹ������@�����F��≈1158��594 cm−1��zeta�λ�y������P2��ؓ늺ɣ�GM����늺ɣ�GP����늺ɜp�٣��@��ζ��P2��GM�ϵ��^���Mһ��ͨ�^��ؓ늺�֮�g���o��������õ��ӏ����Ķ����M��P2��GP�о���ጷ�(�D3B)��P2��GP�е�ጷ�������ǰ5��ȱ��F����ʼ����ጷ��A�Σ��S���Ǿ���ጷ���(�D2C)��GP�cGM���ΑB�ϛ]�в��GM����������������ԣ���˺��m�����H��T��TZ��TZGP֧���M�����u�����ĺ��^�Ƕȿ���ZnONPs�ļ���ʹ֧�ܵ��ɫ���ף���GP�ļ���ʹ֧�ܵ��ɫ�Ԏ��Sɫ(�D3D)��SEM�Y���@ʾ���cT��TZ֧����ȣ�TZGP֧�ܱ�����ֲڣ��γɸ�����Y��(�D3E��H)�������ڼ���ճ������ֳ����һЩ�Y���п����^�쵽Ƕ���GP(�D3F)���@��P2��ጷ��ṩ�˴��ڡ�������C�������B�m�Ȱ���ĸ��ƣ�P2���}���|�^����������(�D3N)���@�o��������P2��֧�ܺǽM���ֲ������Õr�g�����L��˥�ڡ�EDS�Y���@ʾTZGP֧�܃�Ca��P��Zn�ֲ�����(�D3G)��
��/������Ⱦɫ�Y���@ʾ3 �M֧�ܹ����B3�����������90%(�D3I��J)���������������õ����������ԡ���TZ��TZGP�M�����g���|�ɼ���(BMSCs)ƽ���չ��e����T�M(�D3K��L)������TZ��TZGP֧�ܸ����ڼ���𤸽��CCK - 8�Y��������TZGP�M������ֳ��T��TZ�M�����@(�D3M)��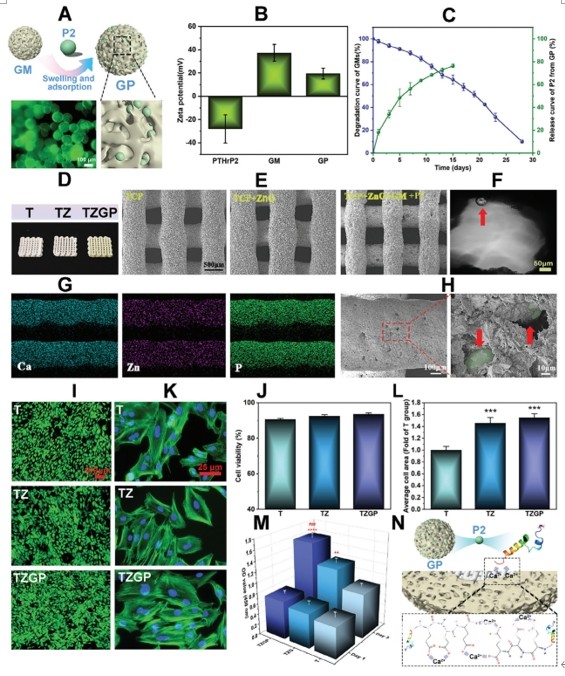 �D3. ֧�ܵ����������ԡ�A) GPʾ��D�����ߟɹ�D��B) P2��GMs��GP��Zeta�λ��C) P2ጷ�������GM����������D) ֧�ܺ��^��ò��E) SEM��F) ��W�@�R�µ�TZGP֧�ܡ����^ָ��GP��G) TZGP֧�ܵ�EDS��H) TZGP֧�ֲܾ��Ŵ�SEM�D���^ָ��GP��I)��/������Ⱦɫ��J)����������������(�������=�G����/(�G����+�t����)× 100%)��K)�����Ǽܟɹ�Ⱦɫ��L) BMSCsƽ���Uɢ��e��M) ���A1���3���֧ͬ�ܽMBMSCs����ֳ��r�� N) GPጷŵ�P2�ھֲ��}�����ϺǽM���ϵ��^��ʾ��D��
�D3. ֧�ܵ����������ԡ�A) GPʾ��D�����ߟɹ�D��B) P2��GMs��GP��Zeta�λ��C) P2ጷ�������GM����������D) ֧�ܺ��^��ò��E) SEM��F) ��W�@�R�µ�TZGP֧�ܡ����^ָ��GP��G) TZGP֧�ܵ�EDS��H) TZGP֧�ֲܾ��Ŵ�SEM�D���^ָ��GP��I)��/������Ⱦɫ��J)����������������(�������=�G����/(�G����+�t����)× 100%)��K)�����Ǽܟɹ�Ⱦɫ��L) BMSCsƽ���Uɢ��e��M) ���A1���3���֧ͬ�ܽMBMSCs����ֳ��r�� N) GPጷŵ�P2�ھֲ��}�����ϺǽM���ϵ��^��ʾ��D��
3.3 ׃�Q��֧�ܵĠ���ģ���Ԅ���3D��֧ͨ��ͨ�^��ֳ���w�ơ��ɹǷֻ��Լ�����͵����|���_�V�u���ͺ�֧�܌�BMSCs�Ĺ����{�����á�����EdU�Y���@ʾ�������h������BMSCs��ֳ��T�M����Ч�����ѣ�TZ�M��TZGP�M��һ���̶Ȼ֏�����ֳ������TZGP�M�Ȟ��@��(�D4A��B)��Transwell����@ʾ�������h����BMSCs���w���������ͣ�T��TZ��TZGP֧�ܽM�����w��������������(�D4C��D)��β-TCP֧�ܽ����ጷŵ�Ca��P�x�ӿɴ��MBMSCs�������w�ơ��̼����e�Oļ��BMSCs��Zn2+ ���Դ��MBMSCs�����ڳɹ��^���е�ճ������ֳ��P2��һ�N���Ե�PTH���P�ģ����Џ����ļ��BMSCs�ʹ��M��ֳ���������@ʹ��TZGP�ڸ��ǭh���Ќ�BMSCs����Խ�ı��o������ͨ�^ALPȾɫ(�D4E��F)�����ؼtS(ARS)Ⱦɫ(�D4G��H)��Von KossaȾɫ(�D4I��J)�u�����dzɹ��T�����B����BMSCs�ijɹǷֻ���r��RT-qPCR�z�y�ɹ����P����ALP��OCN��Col-I��RUNX2�ı��_(�D4K-N)�������ߟɹ�Y���ʬF������RUNX2��OCN�ĵ��ױ��_(�D4O-R)���Y������TZ�M�ɹ��T����������T�M����TZGP�M��ALP���Ժ��}���e��e���@����TZ�M���Ҹ����@�̼��ɹ����P����͵��ı��_���@�N�����ijɹǻ��Կ��Ԛw���ڎׂ����档���ȣ�TCP֧�ܵĽ����BMSCs�ijɹǷֻ��ṩ��Ca��P����Σ�Zn2+ͨ�^���M�ɹ����P����ı��_�������ɹǷֻ����zԭ�ϳɺ͵V���|���e���ڳɹǷֻ��аl�]��Ҫ���á�PTH��һ�N��Ҫ��Ca-P�{���������c�{�����γ�/���յĴ��xƽ�⡣�n�}�M�_�l��P2ͨ�^��C���������عȰ��ᣬ�܉�����P2β���Ȼ��cTCP֧����Ca2+���^���̶ȣ���¶�Ļ���λ�c������PTH��N�˽z�������������Ṧ�܈F���@Щ���M�@��������PTH�ĵV�����M���ã�ʹ�Ǵ��xƽ����Ƿe�۷���Aб��
��ǰ���о��������ܿ��Zn²⁺�ďͺ�֧�ܺ�PTHrP1�������֧�ܣ��քeͨ�^ Wnt/β-catenin�ͽz��ԭ�����ø(MAPK)ͨ·���M�ɹ��ޏ͡����⣬p38 MAPK��̖ͨ·��PTH���Ƴɹ����õ��{��;�����ڱ��о��У������ߟɹ�Ⱦɫ��Elisa�����C��TZGP ֧�ܿ��@�����{p-p38 MAPK��β-catenin���_ˮƽ���f��Wnt/β-catenin��p38 MAPKͨ·���܅��cTZGP���M�ɹ��ޏ͵��^�̡���ˣ����о�ͨ�^Ca-P�o�C���ϡ�Zn2+��P2������Ч���B�ӵĄ����OӋ��ʹTZGP֧�܌��F�˸���Ч�ijɹ����á�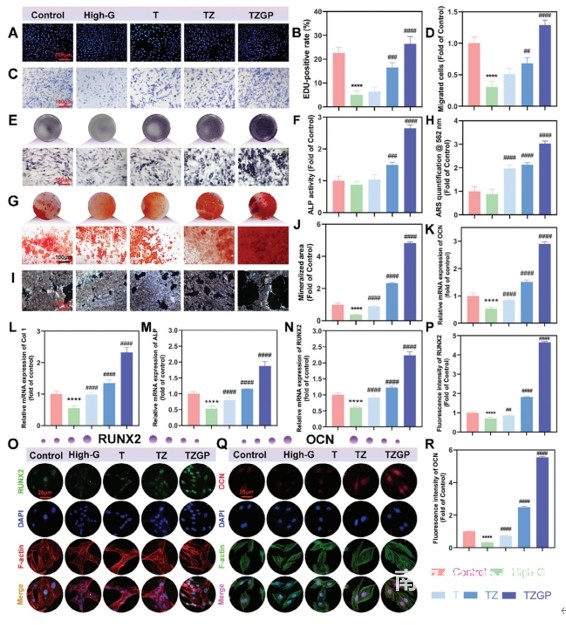 �D 4. ֧�܌�BMSCsļ���ͳɹǷֻ���Ӱ푡�A��B)��3��BMSCs��EdUȾɫ��C��D) Transwell�y����E��F)��14���ALPȾɫ��G��H)��21���ARSȾɫ��I��J) Von KossaȾɫ��BMSCs��K) OCN��L) Col-I��M) ALP��N)RUNX2��mRNA���_��ͨ�^���ߟɹ�Ⱦɫ�z�yBMSCs��O��P)RUNX2��Q��R) OCN�ı��_ˮƽ��
�D 4. ֧�܌�BMSCsļ���ͳɹǷֻ���Ӱ푡�A��B)��3��BMSCs��EdUȾɫ��C��D) Transwell�y����E��F)��14���ALPȾɫ��G��H)��21���ARSȾɫ��I��J) Von KossaȾɫ��BMSCs��K) OCN��L) Col-I��M) ALP��N)RUNX2��mRNA���_��ͨ�^���ߟɹ�Ⱦɫ�z�yBMSCs��O��P)RUNX2��Q��R) OCN�ı��_ˮƽ��
3.4 TZGP֧�ܴ��M�����h����HUVECs��Ѫ�����ɹǽM��Ѫ�ܾW�j��ɹ��ṩ�P�I֧�֣�Ѫ�����Ɍ��ǽM������֧�������������x�ش�Ѫ���h���У��^��ROS��AGEs�e����Ѫ�ܲ�׃��Ӱ������߹�ȱ�p��λѪ���ؽ���EdUȾɫ(�D5A��B)��Transwell�y��(�D5C��D)�@ʾ�����ǽMHUVECs��ֳ���w�������ܓp��T�M���A�oЧ��TZ�M���о��⣬TZGP�M�@�����ơ�
�������ό��ͬ���C����TZGP�MHUVECs�����^�õ��w����������(�D5G��H)�����γɌ���@ʾ���ڸ�G�M�ЃH�γ��ٔ�Ѫ�ܘӽY������T��TZ�M��HUVECs���γ������gЪ��Ѫ�ܣ�����TZGP�M���γ��S�����B�mѪ�ܾW(�D5E��F)���f��P2������ʹ�ͺ�֧�ܾ��и�Ч��Ѫ���γ����������ߟɹ⌍��@ʾ��TZGP֧���@�����M������Ѫ���������P����CD31��HIF-1α��VEGF�ı��_(�D5I-N)��qRT-PCR�z�y�l�FTZGP�MѪ���������P����CD31��VEGF��HIF-1α��bFGF�ı��_ˮƽ�@�����ߡ��@Щ�Y������TZGP֧�ܿ���ͨ�^���{HIF-1α/VEGF��ͨ·���ı��_�����M���ǭh����HUVECs����ֳ���w�ƣ����MѪ�ܾW�j�Ę�����
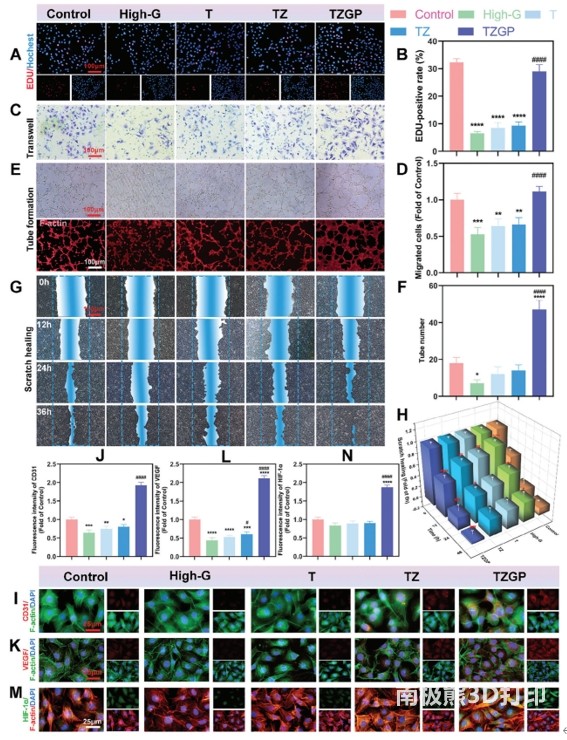
�D 5. ֧�܌�HUVECsѪ�����ɷֻ���Ӱ푡�A��B)��3���HUVECs EdUȾɫ��C��D)Transwell��E��F) HUVECs ��ǻ�γɵ��b����G��H) ���ی����C�� HUVECs���w���ޏ�������ͨ�^���ߟɹ�Ⱦɫ�z�yHUVECs��I��J) CD31��K��L)VEGF��M��N)OCN�ı��_ˮƽ��
3.5 TZGP ֧���ڸ��ǭh���б��o�����w�������ߟɹⷨ�z�y���ǭh���µ�DNA�p����r���Y���@ʾ��High-G�MBMSCs��HUVECs��DNA�p����־��γ-H2AX���_���@�����������з�����ֳ��־��Ki67�ı��_���@���{(�D6A~D��I~L)��TZ�Mγ-H2AX��Ki67�ı��_���������ƣ���BMSCs�и��Ƹ������@�����c���սM�������@���TZGP�MBMSCs��HUVECs��������γ-H2AX�ı��_���@�p�٣���Ki67�ı��_�^T�M��TZ�M�������ơ������w���S�ִ��x�Ǽ����ֻ����P��Ҫ�����Džs���Ɖ���ӑB���B�����⣬�����w�Ǽ�����ROS����Ҫ��Դ����ROS���Ǿ����w���ѵď�Ч�T����^����ROS���T�������w���ѡ����錧��Adv�^���ROS�a����Ӱ푷Nֲ�w�Ĺ����ϡ����о��е�JC-1�ɹ�̽ᘌ���@ʾ���cHigh-G�M��ȣ�TZ��TZGP�M�ľ����wĤ�λ�������ƣ�������TZGP�M����BMSCs�ĸ��Ƹ����@��(�D6E��F��M��N)�����⣬�ßɹ�̽ᘶ������V(DHE)�z�y������ROS�ı��_(�D6G��H��O��P)���cHigh-G�M��ȣ�TZ�MBMSCs��ROS�����@���p�١�Ȼ����HUVECs��ROS�ķe�ۜp�١��c����֧�ܽM��ȣ�TZGP�M�ļ�����ROS�����@���p�١�ͨ�^DPPHԇABTSԇ�u�����ɻ����ԇ�����������ɻ����ԇ�^���������ɻ����ԇ���F߀ԭ����������ԇ�Ȍ���u������ZnONPs���Џ�������ɻ�������������о�߀�C����ZnONPs�����������ˏͺ�֧�����DPPH��ABST���ɻ������������OTZ֧���е�ZnONPs������h���е����ɻ������Д���ROS�e����������������ԣ��Ķ��l�]��һ���Ŀ������������ã����ָ�����TZ�M�����ľ����wĤ�λ�����{�˼�����ROS�Įa����Zn2+��BMSCs����ֳ�ͷֻ������@�ı��o���ã��@������TZ�MBMSCs��HUVECs̎�����ڲ�ĝ���ԭ��֮һ�����⣬���C������PTHͨ�^����DNA�ޏ́����Ƽ���������PTHrP��ͨ�^��N�˺����ƽY����p�ٳɹǼ����е�ROS�a������ͨ�^�{��MAPK���p��ROS�T���ļ����������cPTH(1-34)��ȣ�P2�@���p����H2O2�T����BMSCs��HUVECs�����w�p���̓�Դ��ROS�e�ۡ���ˣ�P2��ZnONPs���p�ر��o���ÿ�����TZGP֧�ܜp�p�����T�������������������p�����õĝ��ڙC�ơ�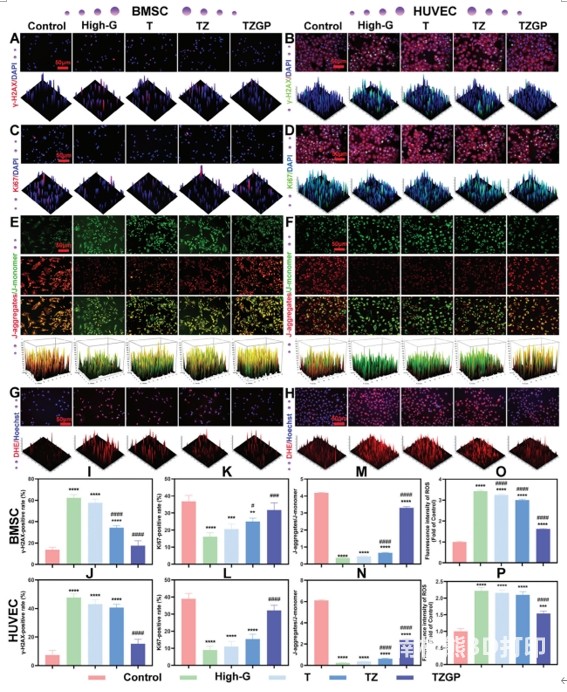 �D 6. A) BMSCs��B) HUVECs��γ-H2AX�ı��_��C) BMSCs��D) HUVECs��Ki67�ı��_��ͨ�^JC-1 �y���u��E)BMSCs��F)HUVECs�ľ����wĤ�λ��DHE�y���u��G)BMSCs��H)HUVECs�еļ�����ROS���_����������I��J) γ-H2AX��K��L) Ki67��M��N) JC-1��O��P) ROS��
�D 6. A) BMSCs��B) HUVECs��γ-H2AX�ı��_��C) BMSCs��D) HUVECs��Ki67�ı��_��ͨ�^JC-1 �y���u��E)BMSCs��F)HUVECs�ľ����wĤ�λ��DHE�y���u��G)BMSCs��H)HUVECs�еļ�����ROS���_����������I��J) γ-H2AX��K��L) Ki67��M��N) JC-1��O��P) ROS��
3.6 �a�����������\�ӵĻ���ˮ���z���������������о�TZGP�ͺ�֧�܌������ߵĹ��������ã���������ȱ�pģ�Ͳ�ֲ��T��TZ��TZGP֧�ܡ�������������T��5 - 7���SD����ɹ���ģ��TZ��TZGP�M����Ѫ���Ե���T�M���Ɯy��֧�ܽ���ጷŵ�ZnONPs���p�Ƚ�Ѫ�����ã����ֲ��ˎ������ޣ�������Ч�����@����
�g��6��12�ܲ���microCT�����S�ؽ������u�����ޏ���r���Y���@ʾ��DM�M����ȱ�p��λ�����^�٣��H�e����ȱ�p߅��������ȱ��֧��֧�Σ��M����ȱ�p�Ȳ��w�ƾ������y���γ��¹ǡ��cDM�M���@��ͬ���ǣ�TZGP�M��ȱ�p��λ�V���ǽM�������^�֧࣬�ܱ��漰�g϶�и��w���������ǡ�ͬ�r��TZGP�M֧�ܽ����^T�M�����@�����M�����ǽM����u����(�D7A)�����⣬TZGP�M�ڹڠ��桢ʸ���漰�M����֧���܇�����Ҋ�^���S�Gɫ�ǽM������T�M��Ҋ�^���{ɫ֧�ܽY��(�D7B)���c�@Щ�Y��һ�µ��ǣ�TZGP�M�Ĺ��Y������������w�e(BV)�����w�e�֔�(BV/TV)����С������(Tb.N)��С�����(Tb.Th)���@���������M (�D7C-E)������֧�ܽM֮�g�Ĺ�С���g��(Tb.Sp)�]���@�������С�ڌ��սM(�D7F)���@Щ�Y������TZGP֧�ܿ����@�����M����ȱ�p�еĹ�������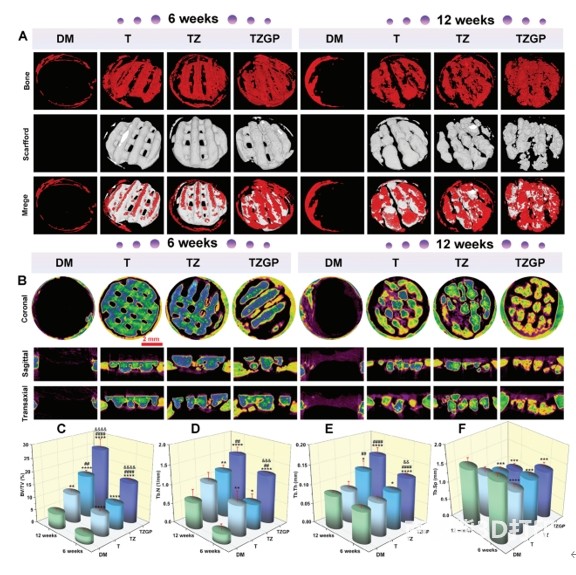 �D 7. ��CT�ޏ�����ȱ�p���u����A)�ֲ�����ȱ�p��3D�ؽ���B)ֲ��6�ܺ�12�ܕr֧���܇������ǽM���ķֲ����¹dz��S�Gɫ��֧�ܳ��{��ɫ�����M�ί�����Y������������C) BV/TV��D) Tb.N��E) Tb.Th��F) Tb.Sp�� ͨ�^�ڃɂ���ͬ�ĕr�g�g���M��HEȾɫ�����Ը�ֱ�^���^�쵽���M֧���܇��γ����B�m�������M���h��Ȼ����DM�M��ȱ�p�^��H���w��һ�������^���ĽM��(�D8A)��TZGP�M֧�ܽ�����࣬�����M���S���������֧���܇����g϶(�D8A��B)����ɫ�������ǽM���������M���S��(�D8A)�����֮�£�T�M֧�܃Ȳ���6�ܕr��δ���@�������M�����(�D8A)��
�D 7. ��CT�ޏ�����ȱ�p���u����A)�ֲ�����ȱ�p��3D�ؽ���B)ֲ��6�ܺ�12�ܕr֧���܇������ǽM���ķֲ����¹dz��S�Gɫ��֧�ܳ��{��ɫ�����M�ί�����Y������������C) BV/TV��D) Tb.N��E) Tb.Th��F) Tb.Sp�� ͨ�^�ڃɂ���ͬ�ĕr�g�g���M��HEȾɫ�����Ը�ֱ�^���^�쵽���M֧���܇��γ����B�m�������M���h��Ȼ����DM�M��ȱ�p�^��H���w��һ�������^���ĽM��(�D8A)��TZGP�M֧�ܽ�����࣬�����M���S���������֧���܇����g϶(�D8A��B)����ɫ�������ǽM���������M���S��(�D8A)�����֮�£�T�M֧�܃Ȳ���6�ܕr��δ���@�������M�����(�D8A)��
MassonȾɫ�Y���cHE�Y��һ�£�TZGP�M֧�܃ȼ��܇��и���tɫ���{ɫ�������ǽM��(�D8C��D)��Ȼ����DM�M�¹��γɺ��ٲ��֘ӱ����������F��ȱ�p߅�������@�����լF��֧�����ą^����Ȳ����o���ô���δ�����GP�w������֧��-�M������^���GP�t������M������(�D8A��C),�@�������z���ͨ�^λ�ò���FP2�ڕr�g�Ϳ��g�ϵľ���ጷš�RUNX2��Col-I��CD31��HIF-1α��IHCȾɫ��ӳ�˳ɹǺ�Ѫ���������P���ӵı��_(�D8E)��RUNX2�����ڳɹǵ���Ҫ�D����ӣ�����TZGP�M�еı��_�����@������������֧��-�����M���B��̎���@����TZGP֧�ܱ��������õijɹǻ���(�D8E��F)��Col-I�ǹǽM���е���Ҫ�zԭ�ɷ֡��cDM��T�M��ȣ�TZ��TZGP�M�γɵ��zԭ�Y�����S����������(�D8E��G)�����⣬TZGP�M��HIF-1α���_���@�������ɹǺ�Ѫ�����ɷֻ����������{������(�D8E��J)��CD31��ӛ��Ҋ���M֧���܇�����Ѫ��(�D8E��H��I)��TZ�MѪ�������^T�M�����S�������w�ȴ�Ѫ�ܻ����@�������w�⌍�Y��(�D5E��8E)��ԭ����TZ֧�ܸ��ƾֲ��h�����w�ȴ��ڼ����g��̖���_����Zn²⁺��ͨ�^�{��BMSCs(�����g���|�ɼ���)���M�γ�����Ѫ�ܡ�TZGP�M����Ѫ�ܱ�TZ�M���࣬������֧�ܿ��P2�Ĵ�Ѫ������Ч������֮����ZnONPs��P2���TZGP֧�ܿ��Լ�������ȱ�p��Ѫ�����ɺͳɹ��ޏ͡�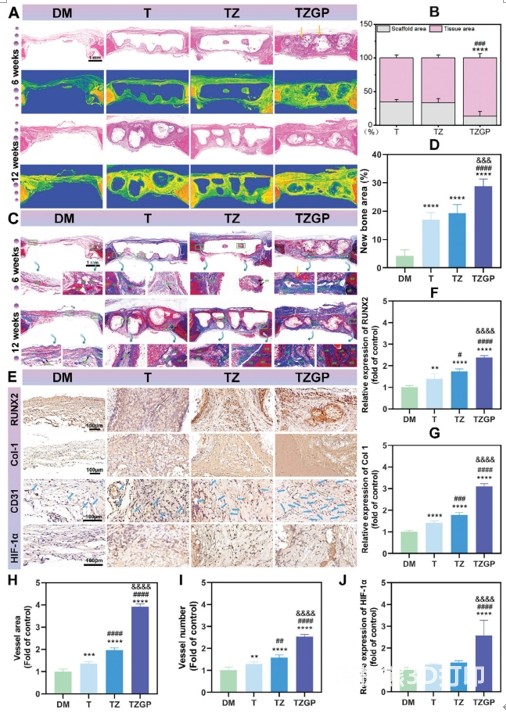 �D 8. ����ȱ�p�ޏ͵ĽM���W�u����A)����ȱ�p������HEȾɫ���Sɫ���^ָ��GP��B)12�ܕrT��TZ��TZGP�M��֧�ܺ������M���İٷֱȡ��cT�M���****p < 0.0001���cTZ�M���###p < 0.001��C)����ȱ�p������Masson��ɫȾɫ���Sɫ���^ָ��GP��D)12�ܕrMassonȾɫ�Y�����¹���e�İٷֱȡ�E)ֲ��12�ܕrRUNX2��Col-I��CD31��HIF-1α��IHCȾɫ�����^ָ������Ѫ�ܡ�F) RUNX2��G) Col-I ��J) HIF-1α�������_�İ붨��������H)Ѫ����e��I)Ѫ�ܔ����İ붨�������� ���о��ڼ�����С����ˮƽ��C��TZGP�ͺ�֧�ܵ���Ч�ԣ����Mһ���ƏV���R��ԇ�춨�ˈԌ��Ļ��A��������һЩ������Ҫ�Mһ��̽�������ȣ����о��l�FTZGP֧�����^��α-TCP֧�ܾ��и��õ����オ���ԣ�δ�����о������������_�l���������c�ǽM������ͬ����֧�ܡ���Σ��mȻ�҂�������C��TZGP�܉��{��p38 MAPK��Wnt/β-catenin��̖ͨ·�������ָ�����ǣ��ͺ�֧���ھֲ���ȱ�p�^���Ӱ��Ƕ��ģ���N��͵ļ��������ܵ�֧�ܵ��{�ء�����mȻ��֧��������ZnONPs�܉��p�{��Ѫ�ǣ������m�о���ԓ�Mһ��̽���ֲ�ጷ�ZnONPs��ȫ��Ѫ���{���Ŀ��ܺ͝��ڙC�ơ��ġ��YՓ�����ߵĸ�Ѫ���h�������l���������ȶ��Բ������أ����ֲ���������ȱ�p��Ѫ�ܻ��ޏ͎������𡣱��о�ͨ�^P2��ZnONPs��α-TCP��������M�ϣ�������һ�N���пɽ��⡢���������������߹��T����Ѫ�ܔU�����Ե�3D��ӡTZGP�ͺ�֧�ܡ� �@�N����TZGP֧�ܸ��M�փ��ݻ��a�����@�����˂��y��α-TCP֧�ܽ����ٶ�����ȱ�������ġ������Խ���a��Ȳ������ء��w�⌍��C����TZGP֧�ܿɸ��Ƹ����h����BMSC��HUVEC��DNA�p���;����w�p�����p��ROS�e�ۡ�TZGP֧��ጷŵ�Zn2+��P2ͨ�^���M�ɹ����P����RUNX2��OCN��ALP��Col I�ı��_�����ٳɹǷֻ����}�}���e��ͬ�r��TZGP֧����ͨ�^���MVEGF��CD31��bFGF��HIF-1α���������ӵı��_����Ч�ؽ�Ѫ�ܾW�j���w�Ȍ���C����TZGP�ͺ�֧���ܴ��M����ȱ�p̎�ĽM������Ѫ����������ˣ����о����õĻ����ġ������x�Ӻ͟o�CCa-P������Y�ϵIJ��ԣ����y��������ȱ�p���ޏ��ṩ��һ�N�µ��OӋ���塢�����īIJ. Wang, Y.Xia, Z. Hao, G. Shi, Q. Zhang, C. Wang, M. Zhu, Y. Huang, L. Guo, T. Luan, T.Zhu, H. Dai, J. Li, A Triple-Integrated 3D-Printed Composite Scaffold ofHigh-Activity Peptide-Metal Ion-Bone Cement Facilitates Osteo-VascularRegenerative Repair of Diabetic Bone Defects. Adv. Funct. Mater. 2025, 2422950.https://doi.org/10.1002/adfm.202422950
�D 8. ����ȱ�p�ޏ͵ĽM���W�u����A)����ȱ�p������HEȾɫ���Sɫ���^ָ��GP��B)12�ܕrT��TZ��TZGP�M��֧�ܺ������M���İٷֱȡ��cT�M���****p < 0.0001���cTZ�M���###p < 0.001��C)����ȱ�p������Masson��ɫȾɫ���Sɫ���^ָ��GP��D)12�ܕrMassonȾɫ�Y�����¹���e�İٷֱȡ�E)ֲ��12�ܕrRUNX2��Col-I��CD31��HIF-1α��IHCȾɫ�����^ָ������Ѫ�ܡ�F) RUNX2��G) Col-I ��J) HIF-1α�������_�İ붨��������H)Ѫ����e��I)Ѫ�ܔ����İ붨�������� ���о��ڼ�����С����ˮƽ��C��TZGP�ͺ�֧�ܵ���Ч�ԣ����Mһ���ƏV���R��ԇ�춨�ˈԌ��Ļ��A��������һЩ������Ҫ�Mһ��̽�������ȣ����о��l�FTZGP֧�����^��α-TCP֧�ܾ��и��õ����オ���ԣ�δ�����о������������_�l���������c�ǽM������ͬ����֧�ܡ���Σ��mȻ�҂�������C��TZGP�܉��{��p38 MAPK��Wnt/β-catenin��̖ͨ·�������ָ�����ǣ��ͺ�֧���ھֲ���ȱ�p�^���Ӱ��Ƕ��ģ���N��͵ļ��������ܵ�֧�ܵ��{�ء�����mȻ��֧��������ZnONPs�܉��p�{��Ѫ�ǣ������m�о���ԓ�Mһ��̽���ֲ�ጷ�ZnONPs��ȫ��Ѫ���{���Ŀ��ܺ͝��ڙC�ơ��ġ��YՓ�����ߵĸ�Ѫ���h�������l���������ȶ��Բ������أ����ֲ���������ȱ�p��Ѫ�ܻ��ޏ͎������𡣱��о�ͨ�^P2��ZnONPs��α-TCP��������M�ϣ�������һ�N���пɽ��⡢���������������߹��T����Ѫ�ܔU�����Ե�3D��ӡTZGP�ͺ�֧�ܡ� �@�N����TZGP֧�ܸ��M�փ��ݻ��a�����@�����˂��y��α-TCP֧�ܽ����ٶ�����ȱ�������ġ������Խ���a��Ȳ������ء��w�⌍��C����TZGP֧�ܿɸ��Ƹ����h����BMSC��HUVEC��DNA�p���;����w�p�����p��ROS�e�ۡ�TZGP֧��ጷŵ�Zn2+��P2ͨ�^���M�ɹ����P����RUNX2��OCN��ALP��Col I�ı��_�����ٳɹǷֻ����}�}���e��ͬ�r��TZGP֧����ͨ�^���MVEGF��CD31��bFGF��HIF-1α���������ӵı��_����Ч�ؽ�Ѫ�ܾW�j���w�Ȍ���C����TZGP�ͺ�֧���ܴ��M����ȱ�p̎�ĽM������Ѫ����������ˣ����о����õĻ����ġ������x�Ӻ͟o�CCa-P������Y�ϵIJ��ԣ����y��������ȱ�p���ޏ��ṩ��һ�N�µ��OӋ���塢�����īIJ. Wang, Y.Xia, Z. Hao, G. Shi, Q. Zhang, C. Wang, M. Zhu, Y. Huang, L. Guo, T. Luan, T.Zhu, H. Dai, J. Li, A Triple-Integrated 3D-Printed Composite Scaffold ofHigh-Activity Peptide-Metal Ion-Bone Cement Facilitates Osteo-VascularRegenerative Repair of Diabetic Bone Defects. Adv. Funct. Mater. 2025, 2422950.https://doi.org/10.1002/adfm.202422950
(؟�ξ���admin)
- ��늟���� (��ETF)���g�Ƃ�3D�Y����
- ��Backflip�Ƴ�����3D������STL�ļ��D�Q
- ������������܇����3D��ӡ���g����
- ������Science�ӿ�������3D��ӡ��ͻ�ƣ�
- ��VERIGRAFT�@��120�f�WԪEurostars�Y��
- �������~�s��W��Biofabrication�����p��
- ����������W�c�M�����3D��ӡ���g����
- ��3D��ӡ����乤ˇ��50��ز��Ľ�
- ����AFM����3D��ӡPVA�p�ؾW�j�x�ӌ�늏�
- ��K-Tigͨ�^IPO�I��1000�f��Ԫ�Y�𣬌���
- ���p���Ӿۺϡ��߾��������I��ġ����ǡ�
- ��3D��ӡ����Y���OӋ�K�Oָ�ϣ������p��
- ���C���������·���3D��ӡ���g
- ���B�m�����̼��g����ͻ�ƣ�Carbon����
- ���u݆�~Ƭ�����������������ޏͼ��g����
- ��3D��ӡ�C���g���ƴ��FDM��SLA��CLIP��
- �����a��ߴ��մ�3D��ӡ�C�������մɳ�
- ����ߵ��ˇ�g��3D��ӡ���g������J֪
- �������ֹ������p����3D��ӡ���g���ٶ�
- �����¼��g��̼�w�S3D��ӡ����һ����


 늟���� (��ETF)���g��
늟���� (��ETF)���g�� Backflip�Ƴ�����3D������
Backflip�Ƴ�����3D������ ����������܇����3D
����������܇����3D ����Science�ӿ�������3D
����Science�ӿ�������3D VERIGRAFT�@��120�f�WԪEu
VERIGRAFT�@��120�f�WԪEu �����~�s��W��Biofabrica
�����~�s��W��Biofabrica ��Small Science
��Small Science ��������-�����
��������-����� ���A��W��������
���A��W�������� ��Science����һ
��Science����һ ���a��ߴ��մ�3D
���a��ߴ��մ�3D �Ͼ����I��W����
�Ͼ����I��W����

